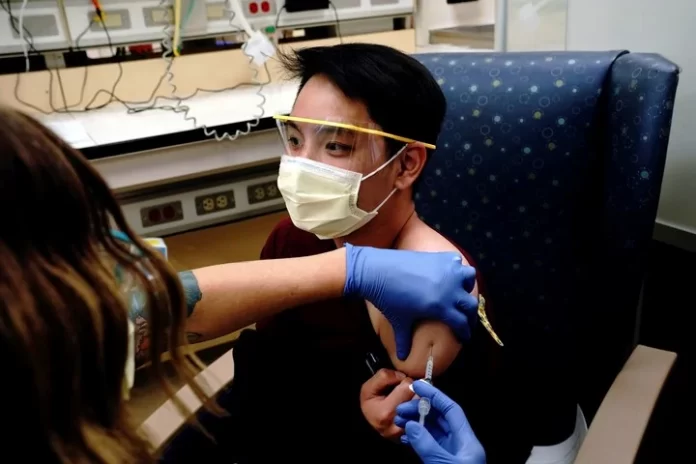
La farmacéutica estadounidense Moderna anunció el lunes resultados positivos de su vacuna contra el coronavirus en niños de entre 6 y 11 años, y tiene previsto presentar «a corto plazo» los datos a los organismos reguladores de todo el mundo para su aprobación.
Los datos de los ensayos clínicos realizados en más de 4.700 niños de esta franja etaria muestran una respuesta inmunitaria «fuerte» en términos de niveles de anticuerpos y un «perfil de seguridad favorable», dijo Moderna en un comunicado.
La empresa de biotecnología informa que, a partir de su análisis, el estudio mostró una sólida respuesta de anticuerpos neutralizantes después de dos dosis de ARNm-1273 con un perfil de seguridad favorable.
«Nos alienta el perfil de inmunogenicidad y seguridad del ARNm-1273 en niños de 6 a menos de 12 años y nos complace que el estudio cumpliera sus criterios de valoración primarios de inmunogenicidad», dijo Stéphane Bancel, director ejecutivo de Moderna.
«Esperamos presentarnos ante los reguladores de todo el mundo y seguimos comprometidos a hacer nuestra parte para ayudar a poner fin a la pandemia de Covid-19 con una vacuna para adultos y niños de todas las edades», añadió.
El estudio se dividió en tres grupos, con más de 4.700 participantes, y demostró una fuerte respuesta inmune en esta cohorte un mes después de la segunda dosis. Además, cumplió con los criterios de valoración de inmunogenicidad coprimaria para niños de seis a menos de 12 años en el KidCOVE.
Moderna apuntó que planea enviar estos datos a la Administración de Drogas y Alimentos de Estados Unidos (FDA), a Agencia Europea de Medicamentos (EMA) y a otros reguladores globales.
La semana pasada Pfizer aseguró que su vacuna es segura y 90,7% efectiva contra el Covid-19 sintomático en niños de 5 a 11 años, en un documento publicado antes de una reunión clave de los asesores de vacunas de la FDA.
En el ensayo, que incluyó alrededor de 2.000 niños, hubo tres casos de COVID-19 en el grupo que recibió la vacuna y 16 casos en el grupo de placebo. En el estudio, el doble de niños recibió la vacuna que el placebo.
Pfizer/BioNTech solicitó la autorización de uso de emergencia de la FDA para un régimen de dos dosis de su dosis de 10 microgramos para niños de 5 a 11 años. Las dos dosis se administrarán con tres semanas de diferencia.
Los expertos aseguran que niños con problemas de salud crónicos serán los más favorecidos con vacunación, pues el coronavirus puede afectarlos al punto de poner en peligro sus vidas o matarlos.
La Comisión Asesora de Vacunas y Productos Biológicos Relacionados de la FDA tiene previsto reunirse mañana para debatir si recomienda la autorización de la vacuna para los niños de 5 a 11 años. Fuente: Clarín// IP


Este medio no se hace responsable ni partícipe de las opiniones vertidas por los usuarios de esta sección. Los comentarios publicados son de exclusiva responsabilidad de sus autores y las consecuencias derivadas de ellos pueden ser pasibles de sanciones legales. Itapúa en Noticias se reserva el derecho de eliminar aquellos comentarios injuriantes, discriminadores o contrarios a las leyes de la República del Paraguay